Kelvin2
Comment définir le Kelvin ?
Définition officielle
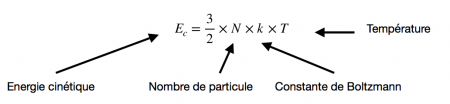
Depuis 2018, le kelvin (symbole K), sur lequel est bâti l’échelle des températures, est défini à partir de constantes fondamentales de la physique . En particulier, le kelvin est défini à partir de la constante de Boltzmann, k. La valeur de la constante k est fixée, et vaut : [math]\displaystyle{ k = 1,380 ~649 ~\times ~10^{-23} m^2 ~kg~s^{-2}~K^{-1} }[/math], Le kilogramme, le mètre et la seconde sont eux-mêmes définis selon d’autres constantes de la physique ([math]\displaystyle{ c,~h,~ \Delta \nu_{Cs} }[/math]) on peut donc déterminer exactement le kelvin à partir de la valeur de k et celles des autres unités.
Définir le kelvin en pratique
En pratique, pour mesurer un kelvin, il faut déterminer avec précision la valeur de la constante de Boltzmann [math]\displaystyle{ k }[/math] grâce à des expérimentations. Il existe à ce jour deux expériences différentes qui permettent de mesurer [math]\displaystyle{ k }[/math] avec une très grande précision et d'une façon assez simple pour les scientifiques. Ces méthodes officielles sont reconnues par le Comité international des poids et mesures (CIPM) qui valide les moyens de définir les unités telles que le kelvin.
- La première méthode reconnue est la thermométrie primaire. Elle consiste à utiliser un thermomètre basé sur des phénomènes physiques connus (la vitesse du son dans un gaz par exemple). Ces phénomènes font intervenir des équations qui relient directement la température aux autres grandeurs (Volume, Pression, etc.) fixées ou mesurées, sans l'aide d'autres constantes fondamentales. C'est de cette manière que l'on peut déterminer la constante de Boltzmann [math]\displaystyle{ k }[/math].
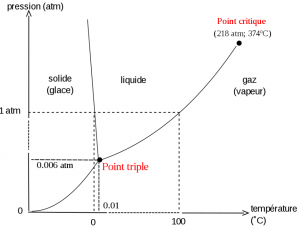
- La deuxième méthode reconnue est celle des échelles de température. Cette méthode utilise les "points fixes" de températures, c'est-à-dire les températures pour lesquelles il se passe un phénomène physique connu (lorsque l'eau liquide devient de la glace par exemple). Pour cela on sélectionne une liste de phénomènes physiques (liés à des changements d'états) auxquels on attribue des températures fixes, puis on crée l'échelle des températures grâce à ces phénomènes et des formules mathématiques.
Histoire du kelvin

C'est au XIXème siècle que le physicien britannique Sir William Thomson (lord Kelvin) introduit la notion de température thermodynamique, qui est basée sur l'existence d'un zéro absolu (0K) et est lié à l'agitation des particules.
Depuis 1954 et jusqu'en 2018, le kelvin était défini à partir du point triple de l'eau, noté [math]\displaystyle{ T_{TPW} }[/math] (température pour laquelle l'eau est à la fois solide, liquide et vapeur). Ce point de référence était fixé à la température [math]\displaystyle{ T_{TPW} =273,16 ~K }[/math] duquel on déduisait la valeur d'un kelvin. En pratique on mesurait donc cette température à l'aide d'une cellule point triple de l'eau. Malheureusement, on a remarque que plusieurs cellules fournissaient des valeurs différentes de température car la mesure dépend beaucoup de la composition de l'eau (présence d'impuretés chimiques et caractéristiques de l'eau). Cette échelle de temperature était également peu fiable pour les valeurs de températures très éloignées de celle du point triple de l'eau. Pour toutes ces raisons, les spécialistes de métrologie (science qui étudie les unités) ont décidé de définir le kelvin à partir d'une constante fondamentale et des autres unités.
Différence entre kelvin, degré Celsius et Fahrenheit
Pour les raisons historiques de la définition de la température, on l'exprime souvent en degré Celsius. Selon cette échelle, le 0°C correspond au point de congélation de l'eau, soit 273,15 K (0,1 K de moins que le point triple de l'eau) à pression atmosphérique et 100°C correspondent à la température d'ébullition de l'eau à pression atmosphérique.
On passe donc de la température en kelvin à la température en degré Celsius de la façon suivante : [math]\displaystyle{ t(°C) = T(K) - 273,15~K }[/math] . On ne peut pas passer de l'un à l'autre par un rapport de multiplication, donc le degré celsius n'est pas une vraie unité, bien qu'il soit pratique dans l'utilisation courante.
Le degré Fahrenheit, inventé par Daniel Gabriel Fahrenheit en 1724 est en fait plus vieux que le degré Celsius et le Kelvin. Il est encore utilisé dans certains pays comme les Etats-Unis à cause d'un concours historique de circonstances (pas de raison scientifique). Fahrenheit a déterminé son échelle en prenant la température la plus basse enregistrée dans son pays comme point le plus bas, et la température du corps humain comme point le plus haut. Pour cette échelle, la solidification de l'eau (0°C) est atteinte pour 32°F.
Finalement la relation de conversion entre degré Celsius et degré Fahrenheit est : [math]\displaystyle{ T(°F) = 1,8 \times T(°C) + 32 }[/math]
Outils de mesure de la température

Le thermoscope
Au début du 17e siècle, Galilée comprend que l'air se dilate avec la chaleur, et se contracte avec le froid. Il met alors au point un appareil appelé thermoscope.
Cet appareil est composé d'un ballon en verre relié à un tube fin, en verre également. Le tube est plongé dans un liquide. Lorsque le ballon, et donc l'air qui est à l'intérieur, est chaud, ce dernier se dilate et prend plus de place. Le niveau du liquide (de l'eau) présent dans le tube baisse donc. Lorsque l'air se refroidit, il se contracte, prend moins de place et le niveau du liquide augmente.
Cet appareil ne permet pas de mesurer la température à proprement parler, mais des variations de température.

Thermomètre à alcool
La plupart des thermomètres fonctionnent sur le principe de la dilatation des corps avec la chaleur. Un thermomètre à alcool est composé d'un tube de verre très fin dans lequel se trouve de l'alcool coloré. Lorsque la température augmente, l'alcool se dilate et son niveau dans le tube augmente.
Il faut alors étalonner le thermomètre pour placer les graduations au bon endroit. Pour cela, soit on compare le thermomètre à étalonner à un autre thermomètre, soit on l'étalonne par rapport à un phénomène physique dont on connait la température. Par exemple, dans l'échelle Celsius, la plus utilisée dans la vie courante, on sait que l'eau gèle à 0°C et bout à 100°C. On marque alors ces points, puis il suffit de diviser l'intervalle entre ces deux valeurs de manière régulière.

Thermomètre de Galilée
Le thermomètre de Galilée est composé d'un tube en verre rempli d'un liquide dans lequel se trouvent des flotteurs avec une densité proche de celle du liquide.
Sous chaque flotteur, un médaillon est accroché et indique une température. Lorsque la température de la pièce dans laquelle se trouve le thermomètre augmente, la densité du liquide diminue. Lorsque cette densité devient plus faible que la densité d'un des flotteurs, celui-ci coule. Les flotteurs coulent alors un par un lorsque la température augmente.

Thermomètre à cadran et aiguille
Un thermomètre à cadran et aiguille fonctionne également sur le principe de la dilatation, mais de métaux cette fois. Deux lames de métaux différents sont collées l'une à l'autre, puis enroulées en spirale. Le centre de la spirale est fixé au centre du cadran, et l'extérieur est libre. Comme les deux métaux ont des coefficients de dilatation différents (c'est-à-dire qu'ils ne vont pas se dilater dans les mêmes proportions), la spirale va se déformer lorsque la température change, ce qui va déplacer la pointe extérieure et donc l'aiguille, qui indiquera la température correspondante sur le cadrant.
Thermomètres électroniques
Thermistances
Une thermistance est une résistance qui possède la propriété de varier en fonction de la température. Elles peuvent être utilisées pour des températures allant jusqu'à 300°C.
|
|
Thermocouples
Un thermocouple est un circuit électrique fermé constitué de deux conducteurs faits de métaux différents.
Il fonctionne à partir de deux effets:
- L'effet Seebeck: dans un circuit fermé constitué de deux conducteurs de nature différente, du courant circule s'il y a une différence de température entre les deux jonctions du circuit ;
- L'effet Peltier: si on fait passer un courant dans un tel circuit, la température change.
Ainsi, selon les métaux utilisés, on peut mesurer des températures allant de -270°C à 1820°C .
Infrarouge
Un thermomètre à infrarouge mesure la température d'un objet à partir du rayonnement infrarouge qu'il émet.
|
|
On peut ainsi mesurer des températures sans contact, à distance.
Bibliographie/Webographie
- Laboratoire National de Métrologie et d’Essais. Le SI et la métrologie en France. EDP Sciences, 2019. ISBN : 978-2-7598-2370-3
- Site web de Futura Science. Kelvin [En ligne, consulté en juin 2021] : https://www.futura-sciences.com/sciences/definitions/physique-kelvin-353/
- Site web de l'institut NEEL, CNRS. Thermométrie [En ligne, Consulté en juin 2021] : http://neel-2007-2019.neel.cnrs.fr/spip.php?rubrique953
- CNRS, Le journal. Le SI reprend sa température. Christophe Daussy, 2018. [En ligne, consulté en juin 2021] : https://lejournal.cnrs.fr/billets/le-si-reprend-sa-temperature
- Météo France: La mesure de la température. [en ligne]. Version 1.0 - décembre 2008. [En ligne, consulté en juin 2021]. http://files.meteofrance.com/files/education/temperature.pdf
- Version numérique du dictionnaire Larousse. Sir William Thomson, lord Kelvin. [En ligne, consulté en juin 2021]. https://www.larousse.fr/encyclopedie/personnage/sir_William_Thomson/146665
- Site web Archi7, les sciences de tous les jours. Petite histoire des échelles de température. [En ligne, consulté en juin 2021] : https://www.archi7.net/J34/index.php/notions/77-petite-histoire-des-echelles-de-temperature
- Site web AlgoRythmes, mathématiques vivantes. Les degrés Fahrenheit, d'où ça vient ?.Sonia Marichal, 2009 [En ligne, consulté en juin 2021] : http://algorythmes.blogspot.com/2009/06/les-degres-fahrenheit-dou-ca-vient.html