« Mole » : différence entre les versions
m (→Bibliographie/Webographie : rédaction références bibliographiques) |
Aucun résumé des modifications |
||
| Ligne 2 : | Ligne 2 : | ||
<div align="justify"> | <div align="justify"> | ||
{{En bref| La '''mole''' ('''mol''') est l'unité du système international (SI) pour la '''quantité de matière'''. <br> Comme la paire ou la dizaine qui désignent respectivement 2 et 10 objets, une mole désigne un "groupe" de | {{En bref| La '''mole''' ('''mol''') est l'unité du système international (SI) pour la '''quantité de matière'''. <br> Comme la paire ou la dizaine qui désignent respectivement 2 et 10 objets, une mole désigne un "groupe" de <math>6,02214040×10^{23}</math> objets, soit environ '''602 214 milliards de milliards''' d'objets. Ce nombre, appelé '''nombre d'Avogadro''', correspond au nombre d'atomes présents dans 12g de carbone 12. Il est utilisé en physique et en chimie pour compter des entités élémentaires (atomes, molécules, isotopes...) }} | ||
On peut calculer le nombre de moles d'un substance que l'on a avec la formule suivante: <math>n=\frac{m}{M}</math> où <math>n</math> est le nombre de moles, <math>m</math> la '''masse totale''' de la substance, exprimée en grammes, et <math>M</math> la '''masse molaire''' du composé, exprimée en grammes par mol (<math>g.mol^{-1}</math>). {{Note|La '''masse molaire''' d'un élément est la masse d'une mole de cet élément. }} | On peut calculer le nombre de moles d'un substance que l'on a avec la formule suivante: <math>n=\frac{m}{M}</math> où <math>n</math> est le nombre de moles, <math>m</math> la '''masse totale''' de la substance, exprimée en grammes, et <math>M</math> la '''masse molaire''' du composé, exprimée en grammes par mol (<math>g.mol^{-1}</math>). {{Note|La '''masse molaire''' d'un élément est la masse d'une mole de cet élément. }} | ||
Dernière version du 10 avril 2017 à 08:12
On peut calculer le nombre de moles d'un substance que l'on a avec la formule suivante: [math]\displaystyle{ n=\frac{m}{M} }[/math] où [math]\displaystyle{ n }[/math] est le nombre de moles, [math]\displaystyle{ m }[/math] la masse totale de la substance, exprimée en grammes, et [math]\displaystyle{ M }[/math] la masse molaire du composé, exprimée en grammes par mol ([math]\displaystyle{ g.mol^{-1} }[/math]).
|
|
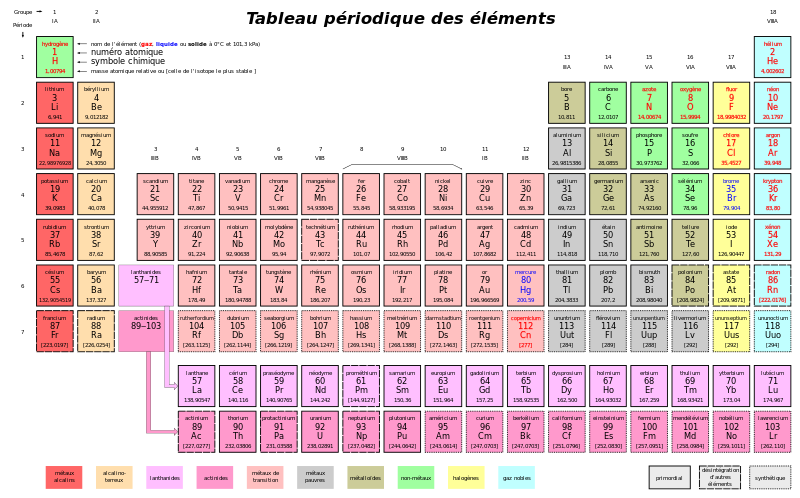
Dans le tableau périodique, comme celui que l'on peut voir ci-dessous, la masse atomique est indiquée. La masse atomique correspond à la masse d'un atome, mesurée en unités de masse atomique (u.m.a. ou u). L'unité de masse atomique est définie ainsi: 12u.m.a. correspondent à la masse d'un atome de carbone 12.
La valeur de la masse d'une mole d'un élément exprimée en grammes, c'est-à-dire de la masse molaire, est la même que la masse atomique du même élément exprimée en u.m.a.
Pour aller plus loin
Dimitri Mendeleiev - Classer les éléments sans les comprendre - e-penser (20min)
Bibliographie/Webographie
BIPM: Résolution 3 de la 14e CGPM, 1971 [en ligne, consulté le 4 juillet 2016]. Disponible sur internet: <http://www.bipm.org/fr/CGPM/db/14/3/>
HECHT, Eugene. Physique. Traduction de la 1ère édition américaine. éd. De Boeck Université, 1999. 1304 p. ISBN 2-7445-0018-6